Ciclo termodinâmico
[[Categoria:!Artigos que carecem de notas de rodapé desde Erro de expressão: Operador < inesperado]]
Um ciclo termodinâmico se constitui de qualquer série de processos termodinâmicos tais que, ao transcurso de todos eles, o sistema regresse a seu estado inicial; ou seja, que a variação das grandezas termodinâmicas próprias do sistema seja nula.
Um fato característico dos ciclos termodinâmicos é que a lei da conservação de energia dita que: a soma de calor e trabalho recebidos pelo sistema deve ser igual à soma de calor e trabalho realizados pelo sistema.
Trabalho
Num ciclo termodinâmico, o trabalho (W) realizado é, por definição, equivalente à área interna ao ciclo num diagrama pressão x volume:
- <math> \text{(1)} \qquad W = \oint P \ dV </math>
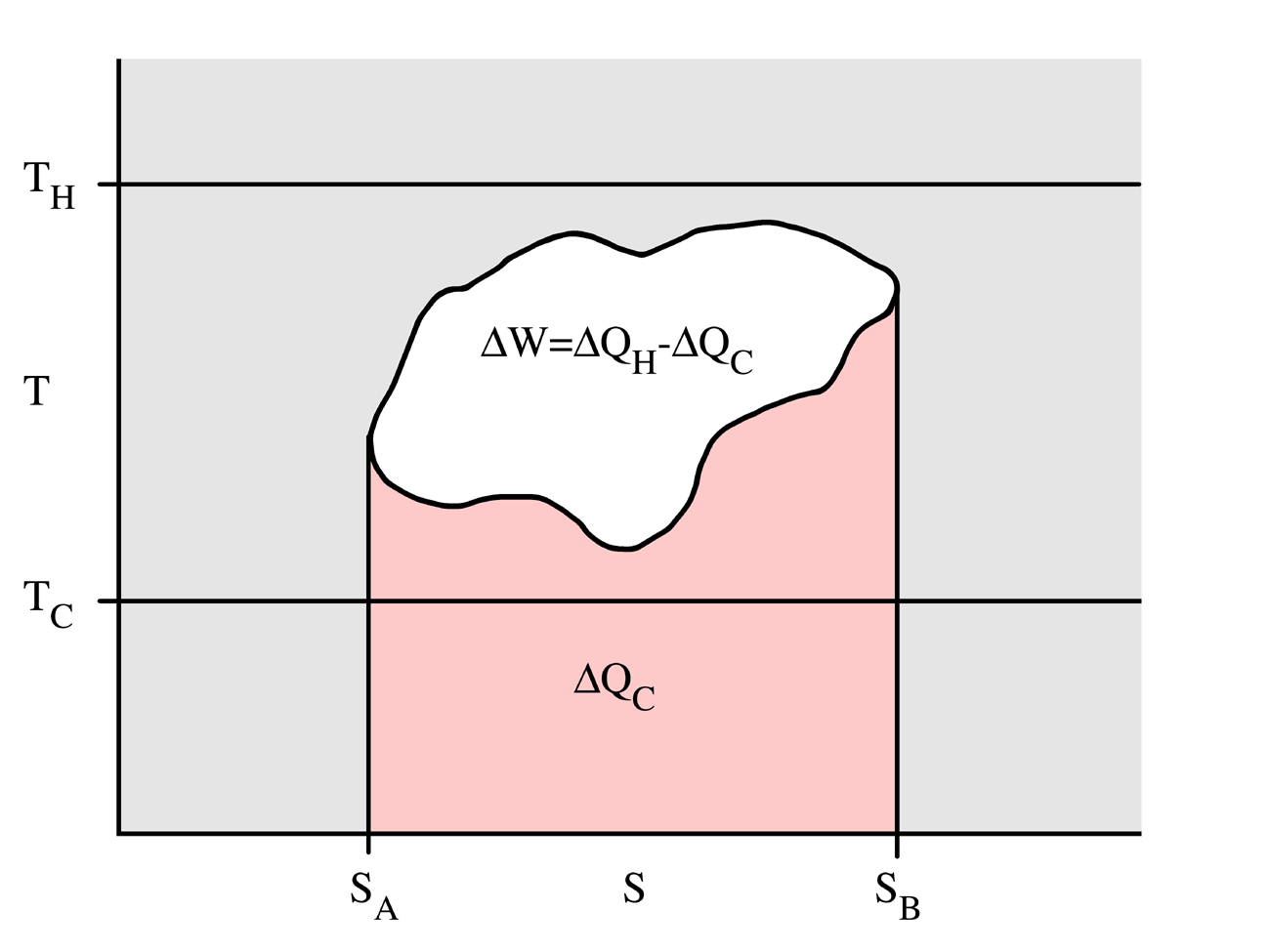
O trabalho equivale à diferença entre o calor absorvido e o calor rejeitado no ciclo:
- <math> \text{(2)} \qquad W = Q = Q_{a} - Q_{r} </math>
É pertinente notar que o sentido em que ocorrem os processos, ou seja as direções das setas no diagrama pressão x volume, determinam se o trabalho é positivo ou negativo. Estas duas possibilidades discriminam os ciclos em duas classes principais: os ciclos motores que transformam calor em trabalho positivo e as bombas de calor que consomem trabalho, permitindo absorver calor de fonte fria.
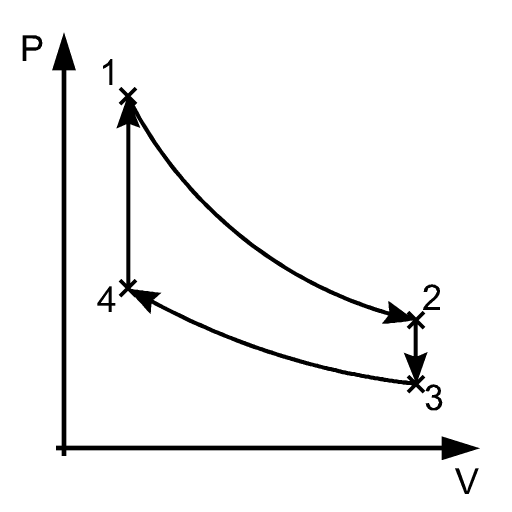
Segue um exemplo de trabalho mecânico realizado em um motor de calor, composto por 4 processos termodinâmicos:
- <math> \text{(3)} \qquad W = W_{1\to 2} + W_{2\to 3} + W_{3\to 4} + W_{4\to 1} </math>
- <math> W_{1\to 2} = \int_{V_1}^{V_2} P \, dV, \, \, \text{negativo, trabalho realizado no sistema} </math>
- <math> W_{2\to 3} = \int_{V_2}^{V_3} P \, dV, \, \, \text{trabalho nulo se V2 for igual a V3} </math>
- <math> W_{3\to 4} = \int_{V_3}^{V_4} P \, dV, \, \, \text{positivo, trabalho realizado no sistema} </math>
- <math> W_{4\to 1} = \int_{V_4}^{V_1} P \, dV, \, \, \text{trabalho nulo se V4 for igual a V1} </math>
Se nenhuma mudança de volume ocorrer nos processos 4->1 e 2->3, a equação (3) se torna:
- <math> \text{(4)} \qquad W = W_{1\to 2} + W_{3\to 4} </math>
Obtenção de trabalho
A obtenção de trabalho a partir de duas fontes térmicas com diferença de temperatura é empregada para produzir movimento, por exemplo, nos motores ou nos alternadores empregados na geração de energia elétrica. O rendimento é o principal parâmetro que caracteriza um ciclo termodinâmico e é definido como o trabalho obtido dividido pelo calor gasto no processo, em um mesmo tempo de ciclo completo, se o processo é contínuo.
Este parâmetro é diferente segundo os múltiplos tipos de ciclos termodinâmicos que existem, mas é limitado pelo fator ou rendimento (eficiência) do ciclo.
Ciclos
Ciclos termodinâmicos são a base de operação de motores de calor, que operam grande parte dos veículos automotores. Ciclos termodinâmicos podem ser divididos de acordo com o tipo de motor de calor que eles desejam modelar. Os ciclos mais comuns são os que modelam motores de combustão interna. O ciclo de Otto modela motores à gasolina, O ciclo Diesel modela motores à diesel. Ciclos que modelam motores de combustão externa incluem o ciclo de Brayton, que modela turbinas de gás, e o ciclo de Rankine, que modela turbinas de vapor.
Ciclo Ideal
Um ciclo ideal consiste em:
- Topo e base do ciclo: par de processos isobáricos
- Esquerda e direita do ciclo: par de processos isocóricos
Ciclos inversos e Bomba de calor
Um ciclo termodinâmico inverso busca o contrário do ciclo termodinâmico de obtenção de trabalho. Aporta-se trabalho externo ao ciclo para conseguir que a transferência de calor se produza da fonte mais fria à mais quente.
Ciclos de bomba de calor são modelos termodinâmicos aplicados em bombas de calor e refrigeradores.A diferença entre os dois é que bombas de calor são feitas para manter um local quente, enquanto refrigeradores são feitos para refrigerá-lo. O ciclo de refrigeração mais simples é o de compressão de vapor, que modela sistemas usando refrigeradores que mudam de fase.Ciclos de refrigeração de gás incluem o ciclo de Brayton reverso e o ciclo de Hampsom-Linde.
Ciclos termodinâmicos conhecidos
Na prática, ciclos termodinâmicos idealizados simples são geralmente compostos por quatro prcessos termodinâmicos. A princípio, qualquer processo pode ser usado, no entanto, quando ciclos idealizados são modelados, geralmente se mantém uma das variáveis de instância constante, como nos seguintes processos: processo isotérmico (temperatura constante), processo isobarico (pressão constante), processo isocórico (volume constante), processo isotrópico (entropia constante) ou processo entalpico (entalpia constante). Geralmente processos adiabáticos (onde não a troca de calor) também são usados. Alguns exemplos de processos termodinâmicos e os processos que os compõem:
| Ciclo | Processo 1-2 (Compressão) |
Processo 2-3 (Adição de Calor) |
Processo 3-4 (Expansão) |
Processo 4-1 (Rejeição de calor) |
Notas |
|---|---|---|---|---|---|
| Ciclos geralmente com Combustão externa - ou ciclos de bomba de calor: | |||||
| Bell Coleman | adiabático | isobárico | adiabático | isobárico | Ciclo de Brayton reverso |
| Carnot | isotrópico | isotermo | isotrópico | isotermo | |
| Ericsson | isotermo | isobárico | isotermo | isobárico | o segundo Ciclo Ericsson de 1853 |
| Rankine | adiabático | isobárico | adiabático | isobárico | Motor a vapor |
| Scuderi | adiabático | pressão e volume variáveis | adiabático | isocórico | |
| Stirling | isotermo | isocórico | isotermo | isocórico | |
| Stoddard | adiabático | isobárico | adiabático | isobárico | |
| Ciclos geralmente com Combustão interna: | |||||
| Brayton | adiabático | isobárico | adiabático | isobárico | Motor de jatos A primeira versão de combustão externa desse ciclo é conhecida como o primeiro Ciclo Ericsson de 1833 |
| Diesel | adiabático | isobárico | adiabático | isocórico | |
| Lenoir | isobárico | isocórico | adiabático | Jatos de pulso (Nota: Processo 1-2 realiza ambos rejeição de calor e de compressão) | |
| Otto | adiabático | isocórico | adiabático | isocórico | Motores a gasolina / petróleo |
Referências
- Halliday,D., Resnick,R.,Walker,J.; Física, Vol. 2, Livros Técnicos e Científicos Editora, Rio de Janeiro, 1996
- Tipler, P.A.; Física (Para Cientistas e Engenheiros), Vol.2 , Gravitação Ondas e Termodinâmica, 3a Ed., Livros Técnicos e Científicos Editora S.A., 1995
- Gaspar,A.; Física, Vol. 2, Ondas, Óptica e termodinâmica, 2a Ed., Ática Editora S.A., São Paulo, 2009
- Chaves,A.; Física, Vol. 4, Sistemas Complexos e Outras Fronteiras, 1a Ed., Reichmann & Affonso Ed.,2001