Transformação isobárica
[[Categoria:!Artigos que carecem de notas de rodapé desde Erro de expressão: Operador < inesperado]]

Uma transformação isobárica é uma transformação termodinâmica na qual a pressão permanece constante em um sistema fechado, sistema este que permite trocas de energia, mas não de matéria, entre o sistema e sua vizinhança. Essa transformação também recebe o nome de Lei de Charles e Gay-Lussac. No século XVIII, o físico francês Jacques Alexandre César Charles descobriu essa relação entre volume e temperatura. Seu interesse surgiu a partir da prática do balonismo. Em 1787 formula a lei da proporção direta entre o volume e a temperatura de um gás a pressão constante. Essas conclusões foram comprovadas experimentalmente por Joseph Louis Gay-Lussac no início do século XIX, sendo então oficialmente publicada. O termo deriva da língua grega iso, "igual" e baros, "pressão". O calor transferido para o sistema realiza trabalho e, portanto, altera a energia interna do sistema, conforme a primeira lei da termodinâmica:
<math> Q = \Delta U + W\, </math>
Onde <math>Q</math> é o calor, <math>U</math> a energia interna e <math>W</math> o trabalho feito pelo sistema.
Formalismo
À pressão constante, sendo a temperatura da amostra T e o seu volume V, essa relação pode ser expressa matematicamente por:
<math> V/T = constante </math>
Onde essa constante depende da temperatura em que ocorre a transformação da amostra do gás confinado no recipiente. Essa relação pode ser descrita ainda de outra forma. Se a amostra de gás, a uma temperatura inicial <math>T_i</math>, ocupando o volume <math>V_i</math>, passar a ter temperatura <math>T_f</math> e volume <math>V_f</math>, mantendo sempre a pressão constante, pode-se afirmar que:
<math> V_i/T_i = V_f/T_f </math>
Trabalho
O trabalho realizado por uma transformação isobárica, em um sistema fechado, é definido como:
<math>W = \int \! p \,dV \,</math>
Como a pressão <math> p </math> é constante ela sai fora da integral:
<math>W = p\int \! \,dV \,</math>
A integral de <math> dV </math> é a própria variação do volume <math> \Delta V\ </math>.
<math> W = p \Delta V\, </math>
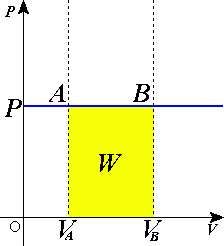
Obs: Vide o diagrama PxV e veja que o valor dessa integral é a própria área W, em amarelo.
Aplicando a Lei dos Gases Ideais, onde segue a relação <math>p= nRT/V</math>, o trabalho torna -se:
<math> W = n\,R\,\Delta T</math>
assumindo que a quantidade de gás permanece constante, por exemplo, não existe uma transição de fase , durante uma reação química. De acordo com o teorema da equipartição, a mudança na energia interna está relacionado com a temperatura do sistema,
<math> \Delta U = n\,c_V\,\Delta T</math>
onde <math> c_V </math> é o calor específico a volume constante.
Substituindo as duas últimas equações na primeira equação, <math> Q = \Delta U + W\, </math>, temos:
<math> Q = n\,c_V\,\Delta T + n\,R\,\Delta T </math>
<math> = n\,(c_V + R)\,\Delta T </math>
<math> = n\,c_P\,\Delta T </math>
onde <math> c_P </math> é o calor específico à pressão constante.
Convenção para o sinal do trabalho:
- Se o volume comprime (<math>\Delta V = V_f - V_i < 0 </math>), então <math>W < 0 </math>. Ou seja, durante a compressão o gás realiza trabalho negativo e o ambiente realiza trabalho sobre o sistema.
- Se o volume aumenta (<math>\Delta V = V_f - V_i > 0 </math>), então <math> W > 0 </math>. Isto é, durante a expansão do gás o trabalho é positivo, ou equivalentemente, o ambiente recebe o trabalho exercido pelo gás.
Ver também
Referências
- HALLIDAY, D., RESNICK,R., WALKER, J., Fundamentos de física. 8ª edição, vol. 2, editora LTC